Le changement climatique met à l’épreuve la résilience des agriculteurs et de leurs cultures. Pour mieux comprendre comment les plantes réagissent à leur environnement dynamique, les scientifiques amplifient les conversations biologiques complexes entre les gènes exprimés dans les cellules végétales. La cartographie de l’expression des gènes est informative, mais les approches traditionnelles de compréhension spatiale de l’expression des gènes sont limitées.

Tatsuya Nobori, biologiste végétal au Salk Institute, étudie les interactions plantes-microbes.
Institut Salk
Dans un récent étude, Tatsuya Noboribiologiste végétal au Salk Institute for Biological Studies, a développé une nouvelle technique permettant de visualiser plusieurs gènes dans le monde végétal interne en 3D.1 Publié dans Plantes naturelles, cette approche ciblée offre un outil prometteur pour comprendre la fonction des types et états cellulaires et leurs interactions avec l’environnement afin d’identifier les caractères bénéfiques pour la sélection végétale de précision.
Les chercheurs utilisent couramment la transcriptomique unicellulaire pour séquencer les cellules individuelles d’un tissu afin de comprendre leurs réponses au stress. Ensuite, ils génèrent des lignées de rapporteurs génétiquement modifiées pour étudier les gènes cibles identifiés lors de l’analyse du transcriptome unicellulaire. La création de ces plantes rapporteuses prend beaucoup de temps et de main d’œuvre, et limite les chercheurs à l’étude d’un seul gène d’intérêt. De plus, les techniques d’imagerie nécessitent de couper le tissu végétal en fines tranches, ce qui entraîne une perte d’informations spatiales.
« Ces limitations entravent considérablement les progrès dans la compréhension de l’analyse spatiale de l’expression des gènes », a expliqué Nobori, qui a dirigé ce travail. Cela a motivé Nobori à développer une nouvelle façon d’examiner les gènes à haute résolution en 3D.
Les découvertes biologiques que PHYTOMap peut potentiellement aider sont les réponses au stress des plantes lorsqu’elles sont exposées à différents stress environnementaux tels que le réchauffement ou le gel des températures et même aux attaques d’agents pathogènes.
– Tatsuya Nobori, Institut Salk d’études biologiques
Pour gagner du temps et étudier des dizaines de gènes à la fois, Nobori a développé une méthode appelée observation ciblée de la carte d’expression génique basée sur l’hybridation végétale (PHYTOMap). S’appuyant sur des technologies d’hybridation et de séquençage in situ, PHYTOMap a visualisé simultanément des dizaines de gènes dans un espace 3D avec un échantillon de tissu entier de Arabidopsis thaliana. « J’ai choisi Arabidopsis comme preuve de concept puisqu’il a été l’organisme modèle pour de nombreux biologistes végétaux et nous a aidés à comprendre les principes fondamentaux de la biologie végétale », a déclaré Nobori.
Nobori ciblé Arabidopsis’ la pointe des racines, une structure essentielle pour étudier la croissance, l’acquisition de nutriments et les interactions avec les microbes du sol. Tout d’abord, il a fixé le tissu entier de l’extrémité de la racine, qui a ancré toutes les molécules d’ARN cibles en place. Ensuite, Nobori a hybridé les molécules d’ARN avec des sondes d’ADN artificielles contenant des codes-barres spécifiques à un gène, qu’il a amplifiés in situ et détectés grâce à la chimie séquence par hybridation. Avec cette technique, il a visualisé des gènes spécifiques, puis a facilement dépouillé les tissus des sondes pour les remplacer par un nouvel ensemble de sondes de gènes cibles.
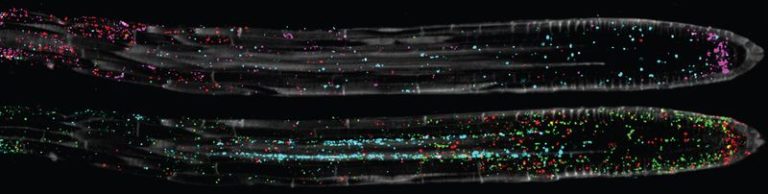
Pour démontrer la capacité de multiplexage de PHYTOMap, Nobori a ciblé 28 gènes à l’extrémité de la racine. Les gènes ciblés comprenaient des gènes marqueurs de types cellulaires connus et d’autres marqueurs candidats identifiés lors du séquençage d’ARN unicellulaire (séquençage d’ARNc) études.2 De plus, PHYTOMap a montré une sensibilité élevée pour les gènes qui présentaient une faible expression et capturaient les principaux types de cellules et stades de développement. Lorsque Nobori a compilé les images, elles ont révélé une toile colorée de gènes Arabidopsis‘ pointe de la racine.
Voir également « Gènes essentiels protégés des mutations«
PHYTOMap a affiché une précision comparable à d’autres techniques basées sur l’imagerie et a détecté avec succès l’ARNm de la protéine fluorescente verte (GFP) dans les types de cellules attendus et les régions de l’extrémité de la racine d’un Arabidopsis modèle. Les chercheurs ont démontré les prouesses de PHYTOMap pour étudier la régulation spatiale des réponses cellulaires dans les tissus végétaux.
« Les découvertes biologiques que PHYTOMap peut potentiellement aider concernent les réponses au stress des plantes lorsqu’elles sont exposées à différents stress environnementaux tels que le réchauffement ou le gel des températures et même aux attaques d’agents pathogènes », a déclaré Nobori. « Les réponses des plantes au stress étant extrêmement hétérogènes, il est très important de comprendre ces réponses à une résolution cellulaire unique avec des informations spatiales. »
Ce travail représente la première approche basée sur l’imagerie des plantes qui nous permet de visualiser les gènes à une résolution subcellulaire, ce qui manquait sur le terrain.
– Stefania Giacomello, Laboratoire de l’Institut royal de technologie et des sciences pour la vie du KTH
Les scientifiques dans le domaine de la transcriptomique spatiale utilisent deux types d’approches : les méthodes basées sur l’imagerie et le séquençage. « Ce travail représente la première approche basée sur l’imagerie des plantes qui nous permet de visualiser les gènes à une résolution subcellulaire, ce qui manquait sur le terrain », a déclaré Stefania Giacomellobiologiste spatial au Laboratoire de l’Institut royal de technologie et des sciences pour la vie du Kungliga Tekniska högskolan (KTH), qui n’a pas participé à cette étude.
En 2017, Giacomello a développé une méthode de séquençage qui complète PHYTOMap en tant qu’outil non ciblé, exploratoire étude de la transcriptomique végétale.3 Cette méthode exploratoire a capturé l’intégralité du transcriptome, mais la résolution n’était pas aussi spécifique que les méthodes basées sur l’imagerie. « C’est à ce moment-là qu’il faut une approche ciblée comme PHYTOMap pour zoomer sur les gènes cibles », a expliqué Giacomello. Grâce à l’imagerie haute résolution, PHYTOMap stimulera les efforts visant à visualiser et à mieux comprendre les interactions dynamiques des gènes des plantes dans des environnements changeants.
Voir également « Siobhán Brady utilise le Big Data pour enquêter sur le développement des usines«
Alors que Nobori se prépare désormais à démarrer son propre laboratoire au laboratoire de Sainsbury, il envisage d’affiner le potentiel multimodal de PHYTOMap. «J’envisage d’équilibrer PHYTOMap de manière à détecter simultanément l’ARN, les protéines et les métabolites afin de maximiser la quantité d’informations obtenues et de mieux comprendre ce qui se passe dans les interactions plante-microbe.»
Les références
- Nobori T, et al. Analyse de l’expression spatiale 3D de gènes unicellulaires multiplexés dans des tissus végétaux à l’aide de PHYTOMap. Plantes Nat. 2023 ; 9 : 1026-1033.
- Shahan R, et al. Une seule cellule Arabidopsis L’atlas des racines révèle les trajectoires de développement des mutants de type sauvage et d’identité cellulaire. Cellule de développement. 2022 ;57 : 543-560.
- Giacomello S, et al. Profilage du transcriptome résolu spatialement chez les espèces végétales modèles. Plantes naturelles. 2017;3:17061.