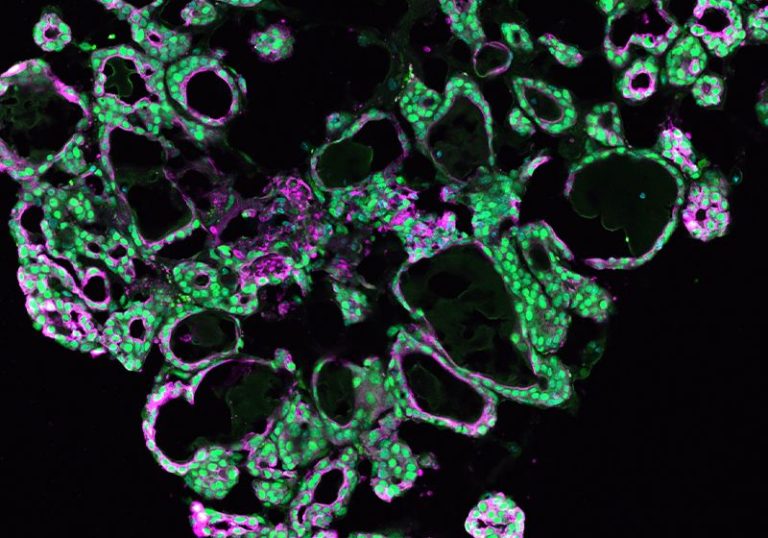
Lles organoïdes cultivés en ab imitent la complexité des organes in vitro et fournissent des informations sur la biologie et les maladies. Les chercheurs ont exploité des organoïdes développés à partir des glandes mammaires ou tumeurs pour étudier le cancer du sein, mais ils manquaient de modèles pour étudier les tissus mammaires développement.1,2
Aujourd’hui, les scientifiques ont identifié un cocktail de produits chimiques pour générer des structures tridimensionnelles ressemblant à des glandes mammaires sécrétant du lait à partir de cellules souches embryonnaires de souris (MESC). Le organoïde modèle, publié dans Cellule de développementpourrait approfondir la compréhension de la manière dont les cellules souches s’engagent dans la lignée mammaire et servent de modèles d’étude sur le cancer du sein.3
« Lorsque nous utilisons des cellules souches embryonnaires, elles subissent tout le processus de différenciation cellulaire programmée, comme cela se produit au cours de l’embryogenèse », a déclaré l’auteur de l’étude. Shyam Sharan, généticien du cancer au National Cancer Institute. « Donc, si vous souhaitez étudier le développement embryonnaire des glandes mammaires, vous pouvez utiliser ce système. »
Pour établir des organoïdes mammaires, l’équipe de recherche a utilisé une approche appelée curation de cellules souches pour générer des organoïdes de la lignée mammaire (CUSTOM). Étant donné que les follicules pileux et les glandes mammaires sont tous deux des appendices cutanés partageant des similitudes de développement, les chercheurs ont utilisé comme point de départ un système organoïde cutané qui produit des follicules pileux.
Les chercheurs ont différencié les MESC en organoïdes cutanés en les traitant avec un cocktail de substances spécifiques. facteurs de croissance.4 Ensuite, ils ont soumis les organoïdes cutanés à un mélange de produits chimiques qui facilitent le développement de la glande mammaire chez l’embryon.5 Les organoïdes résultants contenaient plusieurs types de cellules, notamment des cellules épithéliales, des fibroblastes et des cellules adipeuses. Les chercheurs ont confirmé que ces cellules étaient spécifiques aux lignées mammaires en utilisant le séquençage d’ARN unicellulaire. Ils ont également découvert que ces cellules possédaient des récepteurs pour l’hormone progestérone, caractéristique des glandes mammaires.
Le voyage vers l’établissement des premiers organoïdes mammaires à partir de mESC n’a pas été facile, a déclaré Sharan. Sounak Sahu, un chercheur postdoctoral du laboratoire de Sharan a développé le protocole à partir de zéro. « Nous ne savions pas quoi faire ni quel signal donner avec quelle concentration », a déclaré Sharan. Cela a été encore compliqué par le manque de marqueurs uniques pour confirmer la lignée mammaire des cellules. « Tout marqueur que nous trouverions serait exprimé dans d’autres cellules. Alors, comment savoir si nous allons dans la bonne direction ? il a dit.
Sharan et Sahu ont conçu une expérience pour dissiper tous les doutes. Ils ont traité les organoïdes avec prolactineune hormone responsable de la lactation, et Sharan a été ravie de voir que les organoïdes sécrétaient des protéines du lait, une première pour les organoïdes mammaires dérivés des MESC.6 Enfin, lorsqu’ils ont greffé ces organoïdes dans des coussinets adipeux mammaires débarrassés de leur tissu natif chez des souris nues, les organoïdes se sont reconstitués pour former des glandes mammaires chez la souris.
« Cela a été un problème difficile d’amener les cellules dans un état où l’on pourrait affirmer qu’elles modélisaient réellement l’épithélium mammaire », a déclaré Zev Gartner, chimiste pharmaceutique à l’Université de Californie à San Francisco, qui n’était pas associé à l’étude. « Il y a eu un certain nombre de publications dans ce domaine au cours des cinq ou six dernières années, et celle-ci est de loin celle qui va le plus loin vers l’objectif. »
Gartner, dont l’équipe étudie l’organisation des tissus, a noté que la génération d’organoïdes à l’aide de cellules souches est plus avantageuse que l’utilisation de cellules dérivées de patients, car ces dernières ne sont pas renouvelables et sont plus difficiles à modifier génétiquement. Il a ajouté que la glande mammaire se démarque comme un tissu qui n’a pas été modélisé avec succès à partir de cellules souches embryonnaires. « Maintenant, ce n’est plus le cas », a-t-il déclaré.
Sharan pense que ces organoïdes mammaires aideront les chercheurs à identifier comment les mutations cancérigènes peuvent affecter le développement de la glande mammaire. Il espère également accélérer le calendrier de leur génération à l’avenir, afin que les chercheurs puissent utiliser des organoïdes plutôt que de développer de longs modèles de souris pour modéliser le cancer du sein.
L’équipe prévoit ensuite d’optimiser le processus de croissance d’un plus grand nombre de cellules épithéliales mammaires dans les organoïdes. « Il y a une bonne quantité de tissus accessoires qui accompagnent la différenciation », a déclaré Gartner. « Parvenir à la différenciation au point où la culture est principalement constituée de cellules épithéliales mammaires et du stroma associé est la prochaine grande étape qui, je pense, doit se produire. »
Les références
- Duarte, AA et coll., Organoïdes de tumeur mammaire de souris déficients en BRCA pour étudier la résistance aux médicaments anticancéreux. Méthodes Nat. 2018;15(2):134-140.
- Spina E et Cowin P, Développement embryonnaire de la glande mammaire. Cellule de séminum Dev Biol. 2021;114:83-92
- Sahu, S et.al, La modulation spatio-temporelle des facteurs de croissance dirige la génération d’organoïdes mammaires dérivés de cellules souches embryonnaires de souris multilignées. Cellule de développement. 2024;59(2):175-186.e8.
- Lee J et al., Développement de follicules pileux dans des organoïdes cutanés dérivés de cellules souches pluripotentes de souris. Représentant cellulaire. 2018;22(1):242-254.
- Lee J et al., Peau portant des poils générée entièrement à partir de cellules souches pluripotentes. Nature. 2020;582(7812):399-404
- Al Chalabi M et.al, Physiologie, Prolactine. (Mise à jour le 24 juillet 2023). Dans : StatPearls (Internet). Île au Trésor (FL) : StatPearls Publishing ; 2024